 Воздушно-алюминиевые батареи вырабатывают электричество посредством реакции кислорода в воздухе с алюминием. У них – одно из самых высоких значений плотности энергии среди батарей всех типов, но они все еще не получили широкого распространения из-за сложностей с высокой стоимостью анода и удаления побочных продуктов при использовании традиционных электролитов. Это ограничивает их использование, в основном, до военных отраслей. Однако, у электромобиля с алюминиевыми батареями есть потенциал, восьмикратно превышающий возможности ионно-литиевые аналоги, при этом у них – гораздо меньший вес.
Воздушно-алюминиевые батареи вырабатывают электричество посредством реакции кислорода в воздухе с алюминием. У них – одно из самых высоких значений плотности энергии среди батарей всех типов, но они все еще не получили широкого распространения из-за сложностей с высокой стоимостью анода и удаления побочных продуктов при использовании традиционных электролитов. Это ограничивает их использование, в основном, до военных отраслей. Однако, у электромобиля с алюминиевыми батареями есть потенциал, восьмикратно превышающий возможности ионно-литиевые аналоги, при этом у них – гораздо меньший вес.
Воздушно-алюминиевые батареи относятся к первичным (неперезаряжаемым) элементам. Как только алюминиевый анод истрачивается в ходе реакции с атмосферным кислородом и катодом в водном электролите для формирования гидратного оксида алюминия, батарея больше не может вырабатывать электричество. Однако, есть возможность механической перезарядки батареи с помощью новых алюминиевых анодов, сделанных из переработанного гидратного оксида алюминия. Подобная переработка может стать важной, если воздушно-алюминиевые батареи будут широко применяться.
Электромобили с питанием от алюминиевых батарей последние несколько десятилетий находятся на стадии обсуждения. Гибридизация уменьшит расходы, а в 1989 году было сообщено о проведении дорожных испытаний электромобилей с гибридной воздушно-алюминиевой/свинцово-кислой батареей. В 1990 году в Онтарио была проведена демонстрация гибридного электромобиля класса «минивэн» с питанием от алюминиевой батареи.
В марте 2013 года израильская компания «Phinergy» опубликовала видео демонстрации электромобиля с использованием воздушно-алюминиевых элементов, проехавшего 330 км при помощи специального катода и гидроксида калия. 27 мая 2013 года 10 канал Израиля в выпуске вечерних новостей показал автомобиль с батареей от «Phinergy» в багажнике. Было заявлено, что он может проехать более 2 000 километров (1 200 миль), прежде чем потребуется замена алюминиевых анодов.
Электрохимия
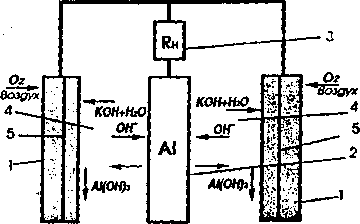
Полуреакция окисления анода выглядит так: Al + 3OH- Al(OH)3 + 3e- + 2.31 В.
Полуреакция восстановления катода выглядит так: O2 + 2H2O + 4e
-
4OH- + 0.40 В.
Общая схема реакции выглядит так: 4Al + 3O2 + 6H2O 4Al(OH)3 + 2.71 В.
За счет этих реакций становится возможной выработка 1,2 В напряжения, что на практике достижимо за счет использования в качестве электролита гидроксида калия. Соленая вода в качестве электролита помогает достичь напряжение в 0,7 В на элемент.
Коммерциализация
Проблемы
Алюминий в качестве «топлива» для автомобилей был изучен Шаохуа Иеном и Гарольдом Найклом. Они пришли к следующим выводам:
«Система воздушно-алюминиевых батарей может вырабатывать достаточно энергии и мощности для дальности пробега и ускорения, аналогичного машинам с ДВС… стоимость алюминия в качестве анода может составлять ниже 1,1 доллара за килограмм, пока продукт реакции подлежит переработке. Общий КПД в ходе циклического процесса в электромобилях с воздушно-алюминиевыми батареями может составить 15 % (нынешний этап) или 20 % (проект), сравнимый с КПД автомобилей с ДВС (13 %). Плотность энергии концепта батареи составляет 1 300 Вт*ч/кг (нынешнее время) или 2 000 Вт*ч/кг (проектный образец). Был проведен анализ цикла долговечности электромобилей с воздушно-алюминиевыми батареями по сравнению с аналогами со свинцово-кислыми и никелевыми гибридными (никелево-марганцовых) батареями. Только электромобили с воздушно-алюминиевыми батареями могут получить диапазон перемещений, сравнимый с аналогами с ДВС. Согласно результатам анализа, данный тип электромобилей является наиболее перспективной по сравнению с автомобилями с ДВС в плане диапазона перемещений, цены покупки, расходов на топливо и срок службы».
Остается решить ряд технических проблем для того, чтобы сделать воздушно-алюминиевые батареи более пригодными для электромобилей. Аноды из чистого алюминия подвержены коррозии со стороны электролита, поэтому алюминий обычно сплавляют с оловом или другими элементами. Гидратная окись алюминия, появляющаяся в результате реакции элемента, формирует гелеобразную субстанцию на аноде и уменьшает выработку электричества. К этой проблеме обращаются на стадии разработки воздушно-алюминиевых элементов. К примеру, были разработаны добавки, формирующий оксид алюминия в виде порошка, а не геля.
Современные воздушные катоды состоят из реактивного слоя углерода с токосъемника с никелевой решеткой, катализатора (к примеру, кобальта) и пористой гидрофобной тефлоновой пленки, предотвращающей утечку электролита. Кислород в воздухе проходит через тефлон, затем – реагирует с водой для создания ионов гидроокиси. Эти катоды работают хорошо, но могут стоить очень дорого.
Стандартные воздушно-алюминиевые батареи имеют ограниченный срок хранения, так как алюминий реагирует с электролитом и производит водород, когда батарея протаивает, хотя этого уже нет в современных образцах. Данной проблемы можно избежать за счет хранения электролита в цистерне вне батареи и перемещения его в батарею при необходимости использования.
Данные батареи, к примеру, можно использовать в качестве резервных батарей в АТС или источников резервного питания. Воздушно-алюминиевые батареи можно использовать для питания ноутбуков и сотовых телефонов, уже сейчас разрабатываются модели для подобного вида работы.
Батареи с алюминием в основе
Были исследованы следующие типы алюминиевых батарей:
1. Хлорно-алюминиевая батарея была запатентована ВВС США в 1970-х годах и разработана, в основном, для использования в военных целях. Они используют алюминиевые аноды и хлор на катодах из графитовой подложки. Для работы им требуются повышенные температуры.
2. Алюминиево-серная батарея крайне заинтересовала американских исследователей, хотя очевидно то, что они все еще далеки от массового производства. В 2016 году в Мэрилендском университете была впервые проведена демонстрация перезаряжаемой алюминиево-серной батареи.
3. Алюминиево-железно-оксидные, алюминиево-медно-оксидные, алюминиево-железно-гидроксидная батареи были предложены некоторыми исследователями для военных ГТС. Их плотность энергии составляет 455, 440 и 380 Вт*ч/кг соответственно.
4. Батарея с алюминием и двуокись марганца использует кислотный электролит. Вырабатываемое напряжение составляет 1,9 В. Другая вариация использует основание (гидроксид калия) в качестве анолита и серную кислоту – в качестве католита. Две части отделены тонкой непроницаемой пленкой во избежание смешения электролита в каждом из элементов в половинах батареи. Эта конфигурация дает напряжение в 2,6-2,85 В.
5. Алюминиево-стеклянная система. Как было сообщено в итальянском патенте от Байокки, в области взаимодействия между силикатным стеклом и алюминиевой фольгой (нет потребности в других компонентах) при температуре, близкой к точке плавления металла, вырабатывается электрическое напряжение вместе с проходящим током, когда система замкнута на активной нагрузке. Феномен впервые был замечен Байокки, а затем – А. Дэлль’Эра и другие коллеги начали исследование и составление характеристики данной электромеханической системы.




